肝细胞癌(Hepatocellular Carcinoma, HCC)是全球范围内最常见的恶性肿瘤之一,其预后与治疗方案的选择高度依赖于肿瘤的生物学行为,其中微血管浸润(Microvascular Invasion, MVI)是一个关键的独立不良预后因素。MVI指在显微镜下于癌旁门静脉分支内发现癌细胞巢,其存在显著增加了术后复发和转移的风险。MVI的确诊通常依赖于术后病理检查,属于有创且滞后性评估。因此,术前无创、精准地预测MVI状态,对于指导个体化治疗策略(如手术范围、辅助治疗决策)具有至关重要的临床价值。
磁共振功能成像技术,特别是扩散加权成像(DWI)及其扩展模型——扩散峰度成像(Diffusion Kurtosis Imaging, DKI),在肝脏肿瘤的微观结构评估中展现出巨大潜力。与传统DWI的单指数模型假设水分子扩散符合高斯分布不同,DKI模型考虑了生物组织内复杂微结构(如细胞膜、细胞器)对水分子扩散的限制,使其扩散行为偏离高斯分布,这种偏离程度用峰度(Kurtosis)来量化。DKI能够提供更丰富的参数,包括平均扩散系数(Mean Diffusivity, MD)和平均峰度(Mean Kurtosis, MK)。其中,MK值反映了组织微观结构的异质性和复杂性,值越高,表明水分子扩散受限越严重,组织越复杂。
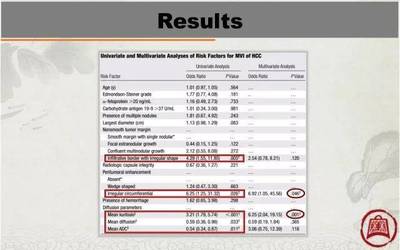
在评估HCC的MVI方面,研究表明,存在MVI的HCC肿瘤往往具有更强的侵袭性、更高的细胞密度以及更紊乱的微血管网络。这些病理特征理论上会导致水分子扩散运动受到更显著的非高斯限制。因此,基于DKI的MK参数被广泛研究用于区分MVI阳性与阴性的HCC。多项研究证实,MVI阳性HCC的MK值通常显著高于MVI阴性者。高MK值可能对应着肿瘤内部更高的细胞增殖活性、更密集的细胞排列以及可能存在的微小坏死灶周围的细胞拥挤区域,这些都间接反映了肿瘤侵袭性增强和MVI风险升高。
为了将DKI技术更高效、标准化地应用于临床科研与实践,专业的影像后处理与分析平台变得不可或缺。MK分析平台正是这样一个集成了图像预处理、模型拟合、参数图生成、感兴趣区(ROI)勾画、特征提取与统计分析于一体的软件系统。其核心工作流程通常包括:
- 数据导入与预处理:平台支持导入原始DKI序列图像,并进行必要的运动校正、配准和噪声过滤,确保数据质量。
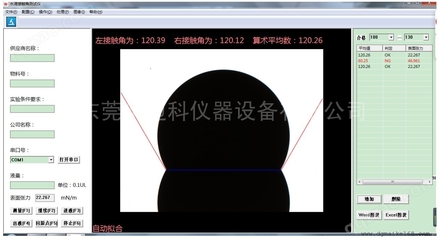
- DKI模型拟合与参数图计算:平台内置算法(如非线性拟合)对每个体素的信号强度与多个b值的关系进行DKI模型拟合,快速生成全脑或全肝的MK图、MD图等参数映射图。这些彩图直观地显示了微观结构异质性在空间上的分布。
- 肿瘤分割与特征提取:医生或研究者可以在平台界面上,基于T2WI、增强扫描等参考图像,在MK图上精准勾画整个肿瘤的ROI。平台自动提取该ROI内的多项特征,如MK平均值、最大值、最小值、百分位数、偏度、峰度(统计意义上的)以及纹理特征(如熵、均匀性)等。这些定量特征构成了评估MVI的影像组学数据基础。
- 统计分析建模:平台可能集成基础统计工具,或支持数据导出,便于研究者将提取的MK特征与临床病理结果(如MVI状态)进行关联分析。通过单因素分析、多因素逻辑回归、机器学习(如支持向量机、随机森林)等方法,构建基于MK及其衍生特征的MVI预测模型,并评估其诊断效能(如灵敏度、特异度、AUC值)。
- 可视化与报告生成:平台提供强大的可视化功能,如多参数图融合显示、直方图分析、特征分布对比图等,并能够生成结构化的分析报告。
利用MK分析平台进行研究,优势在于实现了分析流程的自动化与标准化,减少了人为误差,提高了研究效率与可重复性。未来的发展方向包括:开发更鲁棒的拟合算法以应对肝脏DKI信噪比较低的挑战;整合多参数MRI(如DKI与动态增强DCE-MRI)特征,构建融合模型以提升预测准确性;以及探索基于深度学习的人工智能方法,实现从原始图像到MVI风险分级的端到端自动预测,并推动其向临床决策支持系统的转化。
DKI技术,尤其是其核心参数MK,为无创评估HCC微血管浸润提供了新的重要视角。而专业的MK分析平台作为强大的技术工具,正加速着相关研究成果向临床应用的迈进,有望在未来实现HCC患者术前风险的精准分层与个性化管理。